Die Nutzung von „grünem“ Wasserstoff gilt als entscheidender Baustein für eine klimaneutrale Energiezukunft. Doch für den breiten Einsatz fehlen bislang effiziente und gleichzeitig kostengünstige Katalysatoren für Brennstoffzellen. Ein Forschungsteam der Professur für Elektrobiotechnologie am TUM Campus Straubing und des CNRS Marseille hat nun einen bedeutenden Durchbruch erzielt: Mithilfe eines innovativen polymerbasierten Schutzsystems können empfindliche bakterielle Enzyme erstmals stabil und leistungsfähig in H₂/O₂-Brennstoffzellen eingesetzt werden.
„Grüner“ Wasserstoff wird durch die Elektrolyse von Wasser produziert und ermöglicht eine Stromerzeugung ohne Treibhausgasemissionen. Derzeit basieren jedoch die meisten technischen Katalysatoren auf dem seltenen und teuren Edelmetall Platin. Bakterielle Hydrogenasen, natürliche Enzyme des Wasserstoffstoffwechsels, gelten daher als vielversprechende biologische Alternative. Sie bestehen aus reichlich vorhandenen Metallen wie Eisen – sind jedoch meist extrem sauerstoffempfindlich.
Die Erforschung der enormen Biodiversität dieser Enzymfamilie hat in den letzten Jahren zu neuen Kandidaten mit überraschenden Eigenschaften geführt. Besonders interessant ist eine FeFe-Hydrogenase des anaeroben Bakteriums Clostridium beijerinckii. Sie verfügt über einen natürlichen molekularen Mechanismus, der ihr aktives Zentrum vor Sauerstoff schützt. Allerdings blockiert dieser Schutz gleichzeitig die Fähigkeit des Enzyms, Wasserstoff zu oxidieren – ein zwingender Schritt für den Einsatz in Brennstoffzellen.
Sauerstoffschutz bleibt erhalten
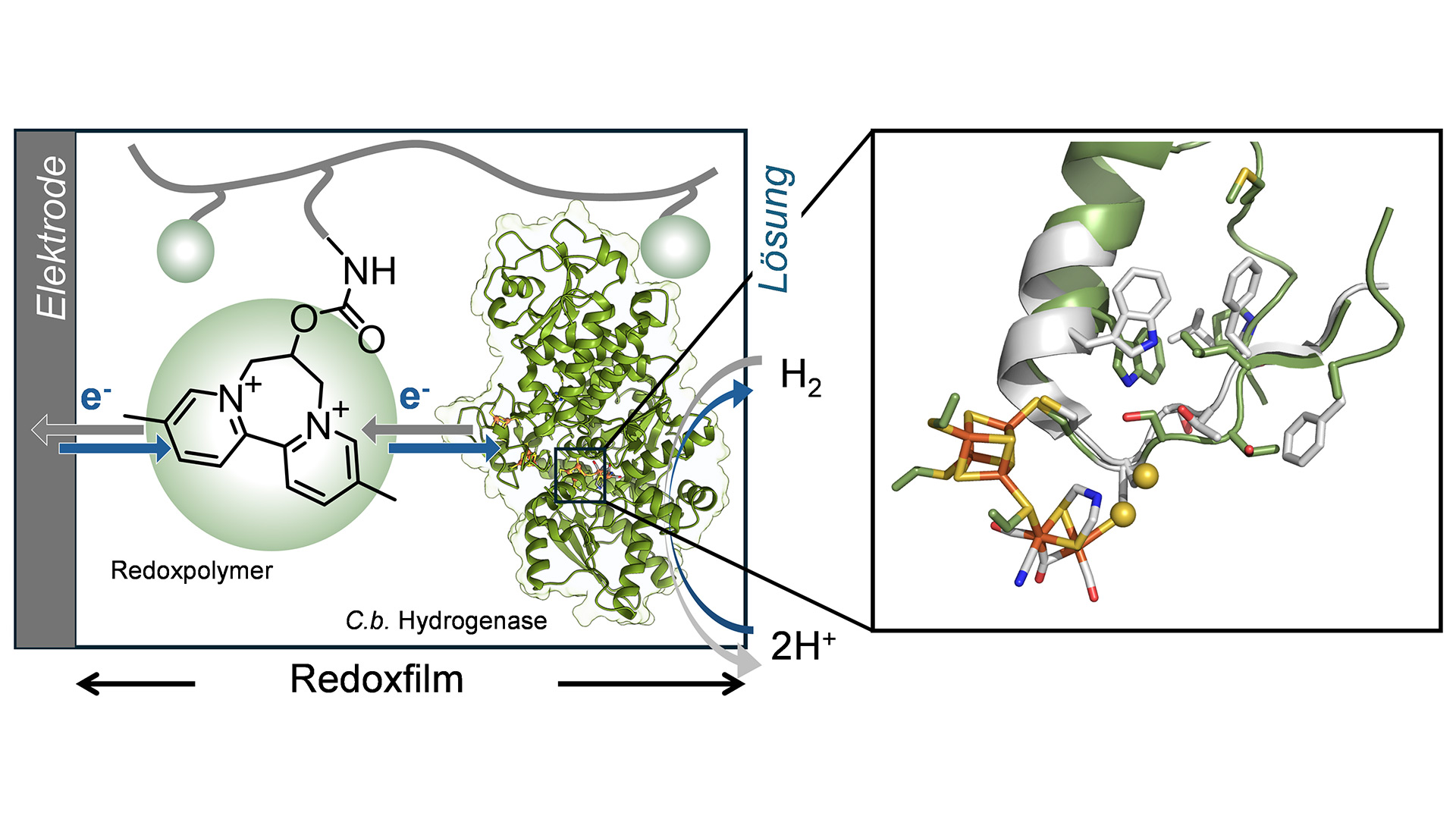
Das Forschungsteam beschreibt nun in der Fachzeitschrift PNAS eine Lösung für dieses Dilemma: Die Hydrogenase wird in einen etwa zehn Mikrometer dicken Film aus einem elektronentransferfähigen, verzweigten Polymer („Dendrimer“) eingebettet. Durch die fein abgestimmten Eigenschaften dieses Redoxpolymers bleibt der Sauerstoffschutz erhalten, während die Wasserstoffoxidationsaktivität reaktiviert wird. So entsteht ein sowohl sauerstoffstabiles als auch hochaktives biokatalytisches System.
Diese patentierte Technologie ist das Ergebnis einer engen Zusammenarbeit zwischen physikalischer Chemie, Polymersynthese, Biochemie und kinetischer Modellierung. Sie ebnet den Weg für neue Generationen biologischer Brennstoffzellen, die nicht nur robuster und langlebiger, sondern auch erheblich kostengünstiger sein können.
Die Studie „Turning the FeFe hydrogenase from Clostridium beijerinckii into an efficient H₂ oxidation catalyst using a redox-active matrix“ wurde von Dawit T. Filmon, Jan Jaenecke, Martin Winkler, Vincent Fourmond, Christophe Léger und Nicolas Plumeré veröffentlicht (PNAS, 2025).